Om Ontozry

Indikasjon
ONTOZRY (senobamat) benyttes som tilleggsbehandling av fokale anfall med eller uten sekundær generalisering hos voksne med epilepsi som ikke er tilstrekkelig kontrollert til tross for tidligere behandling med minst to antiepileptika.1
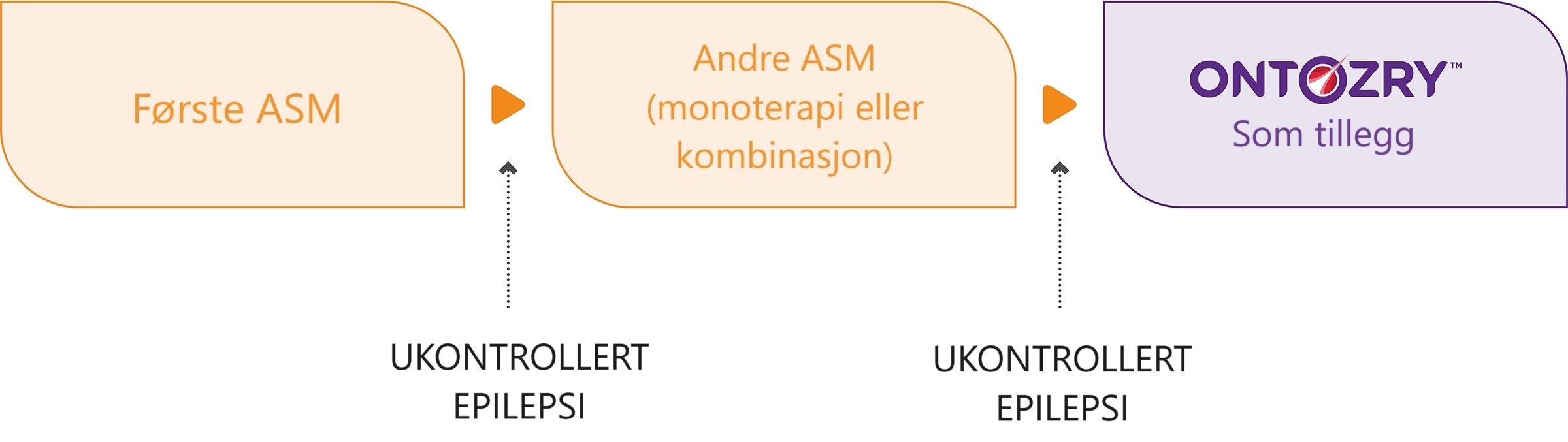
ASM = anti-seizure medication
Virkningsmekanisme for ONTOZRY (senobamat)2,3
ONTOZRY har en dobbel virkningsmekanisme som påvirker både eksitatoriske og inhibitoriske nevrotransmittere.
ONTOZRY har vist seg å redusere gjentakende nevronal avfyring ved å forsterke inaktivering av natriumkanaler og hemme den persistente natrium strømmen.
ONTOZRY er også en positiv allosterisk modulator av undertyper av γ-aminosmørsyre (GABAA)-ionekanalen som ikke binder seg til benzodiazepinbindestedet.
Klikk for forkortet produktinformasjon
Den eksakte virkningsmekanismen ved fokale anfall er ukjent.2
Dosering og titrering av ONTOZRY (senobamat)4
ONTOZRY tas én gang daglig peroralt
- ONTOZRY kan tas med eller uten mat og når som helst på dagen. Skal helst tas ved samme tid hver dag.
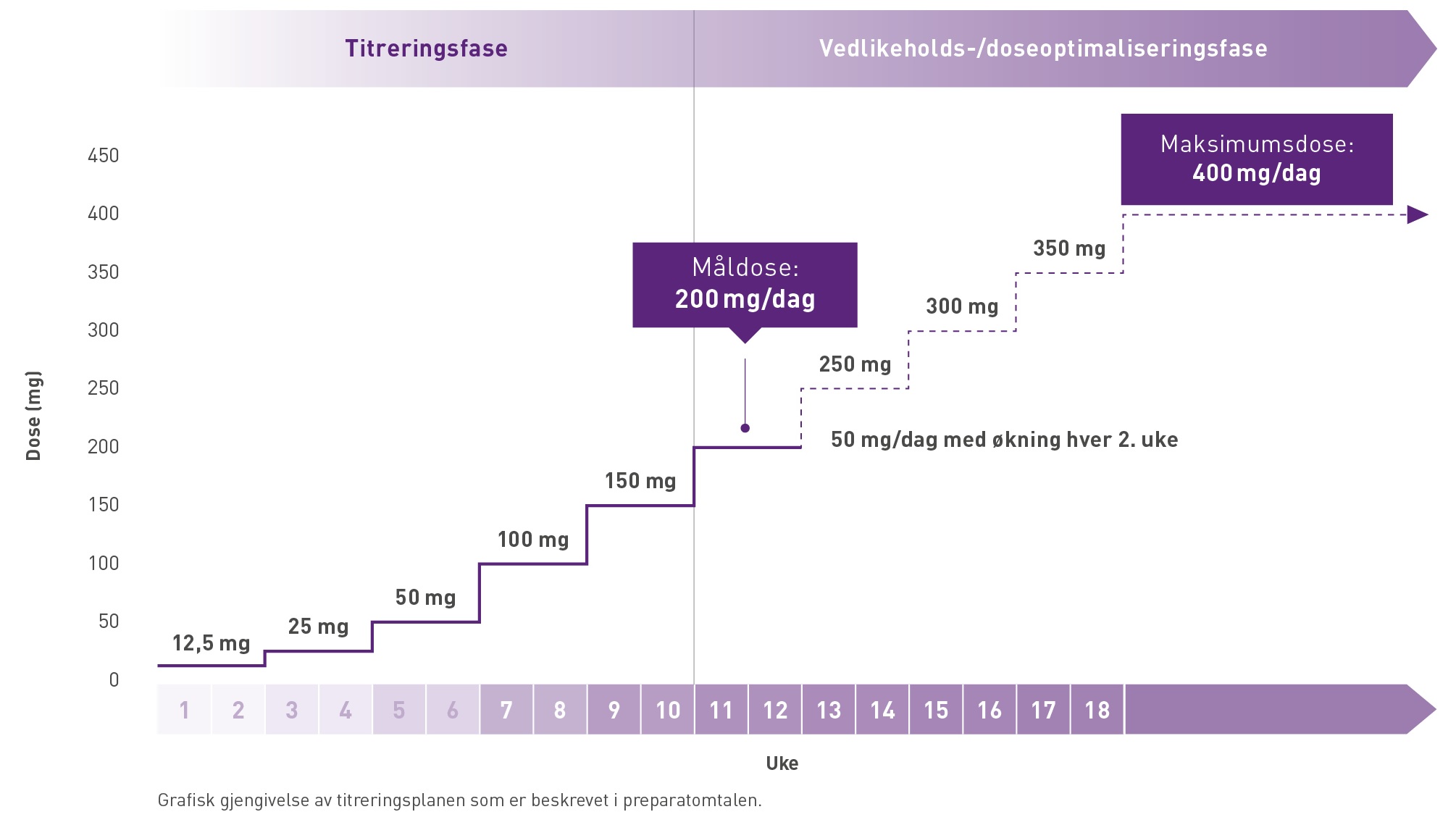
- Den anbefalte startdosen er 12,5 mg/dag.
- Dosen titreres gradvis opp annenhver uke til den anbefalte måldosen på 200 mg/dag.
- Avhengig av pasientens kliniske respons kan dosen titreres opp gradvis til maks. 400 mg/dag.
Figuren nedenfor er en grafisk gjengivelse av det anbefalte titreringsskjemaet i preparatomtalen.
Hva skal pasienten gjøre ved glemt dose av ONTOZRY?
Det anbefales å ta den glemte dosen så snart pasienten husker det, med mindre det er under 12 timer igjen til neste planlagte dose.4
Seponering av ONTOZRY
Seponering bør skje gradvis, dvs. over minst 2 uker, for å redusere risikoen for tilbakevendende anfall, med mindre sikkerhetsproblemer krever umiddelbar behandlingsstopp med ONTOZRY.4
Dosering for personer som er 65 år og eldre4
Ved valg av dose for eldre pasienter bør det utvises forsiktighet, vanligvis med start i det nedre doseringsområdet. Dataene blant eldre er utilstrekkelige for å kunne fastslå om responsen på ONTOZRY er annerledes enn for yngre pasienter. Generelt er det rapportert økt forekomst av visse bivirkninger hos eldre personer som tar antiepileptika. Blant eldre personer er det også høyere forekomst av nedsatt nyre- og leverfunksjon, samtidig sykdom og polyfarmasi.
Nedsatt nyrefunksjon og ONTOZRY4
- Maks. anbefalt dose for pasienter med lett, moderat eller alvorlig nedsatt nyrefunksjon er 300 mg/dag.
- ONTOZRY skal ikke brukes av pasienter med terminal nyresykdom eller pasienter som gjennomgår hemodialyse.
Nedsatt leverfunksjon og ONTOZRY4
- Eksponering for ONTOZRY øker hos pasienter med kronisk leversykdom.
- Maks. anbefalt dose for pasienter med lett eller moderat nedsatt leverfunksjon er 200 mg/dag.
- ONTOZRY skal ikke brukes av pasienter med alvorlig nedsatt leverfunksjon.
Effekt og kliniske data for ONTOZRY (senobamat)2,5,6
Effekten av Ontozry som tilleggsbehandling har blitt undersøkt i to
randomiserte, dobbeltblinde, placebokontrollerte multisenterstudier på voksne pasienter med fokal epilepsi og i en åpen sikkerhetsstudie med mer enn 1900 pasienter.
Studie C017
Studiedesign

Tilpasset av Angelini Pharma fra ref. 5
Primärt endepunkt var ≥50% anfallsreduksjon
En betydelig reduksjon i anfallsfrekvensen ble oppnådd av 56,1 % av pasientene som fikk 200 mg ONTOZRY + standardbehandling*, sammenlignet med placebo + standardbehandling*, der det tilsvarende tallet var 25,5 %.
Ved en dose på 400 mg økte responsraten på 50 % til 64 %, sammenlignet med 25 % for placebo.
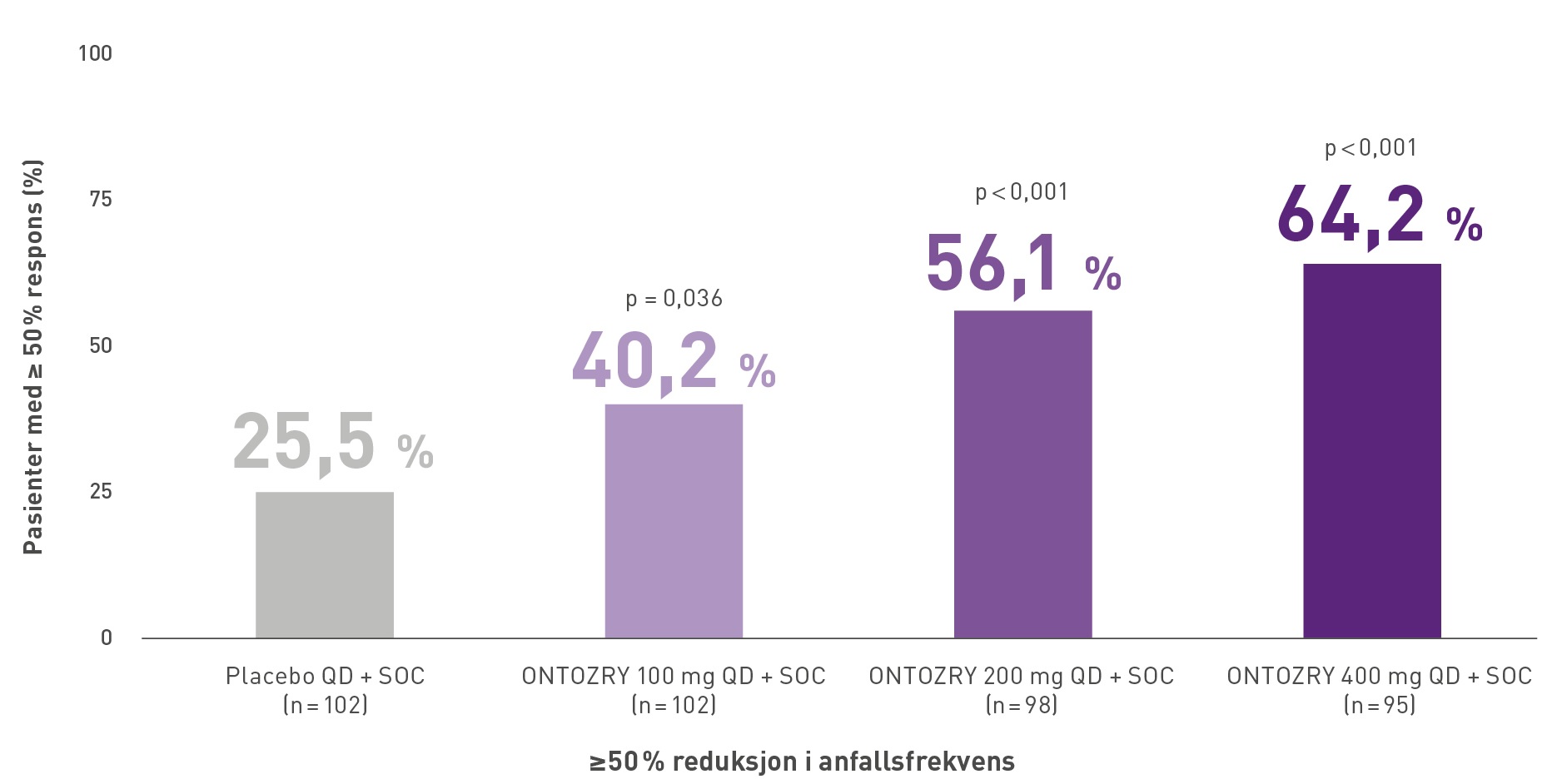
Tilpasset av Angelini Pharma fra ref. 5
QD = én gang daglig; SOC = standardbehandling.
* Standardbehandling var behandling med opptil 3 samtidige antiepileptika.
Pasienter kan bli anfallsfrie med ONTOZRY2,5
28,6 % av pasientene oppnådde en reduksjon i anfallsfrekvensen på ≥75 % med 200 mg ONTOZRY + standardbehandling*, og en reduksjon på 45 % med 400 mg + standardbehandling*.
Henholdsvis 17,3 % og 28,4 % oppnådde en anfallsreduksjon på ≥90 % med henholdsvis 200 mg ONTOZRY + standardbehandling* og 400 mg ONTOZRY + standardbehandling*.
Anfallsfrihet ble påvist hos henholdsvis 11,2 % og 21,1 % av pasientene som fikk henholdsvis 200 mg og 400 mg ONTOZRY + standardbehandling*, sammenlignet med 1 % av de som fikk placebo + standardbehandling*.
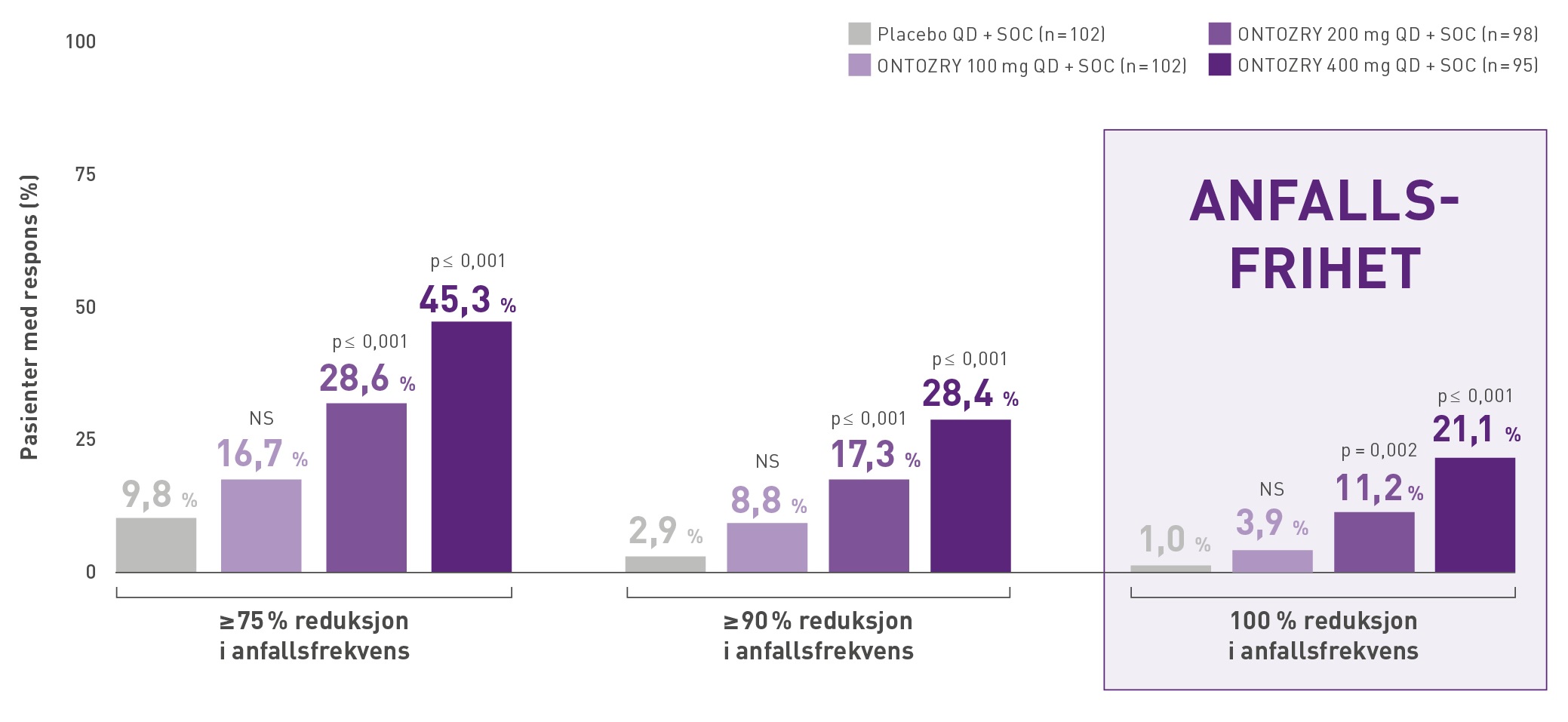
Tilpasset av Angelini Pharma fra ref. 5
Lignende respons ble påvist i undergrupper som lå over eller under median anfallsfrekvens, og i undergrupper med lengre eller kortere sykdomsvarighet enn median varighet.
QD = én gang daglig, SOC = standardbehandling.
* Standardbehandling var behandling med opptil 3 samtidige antiepileptika.
Bivirkninger og sikkerhetsinformasjon for ONTOZRY (senobamat)
Bivirkninger7
ONTOZRY viste god toleranse, med somnolens, svimmelhet, tretthet og hodepine som de vanligst rapporterte bivirkningene.
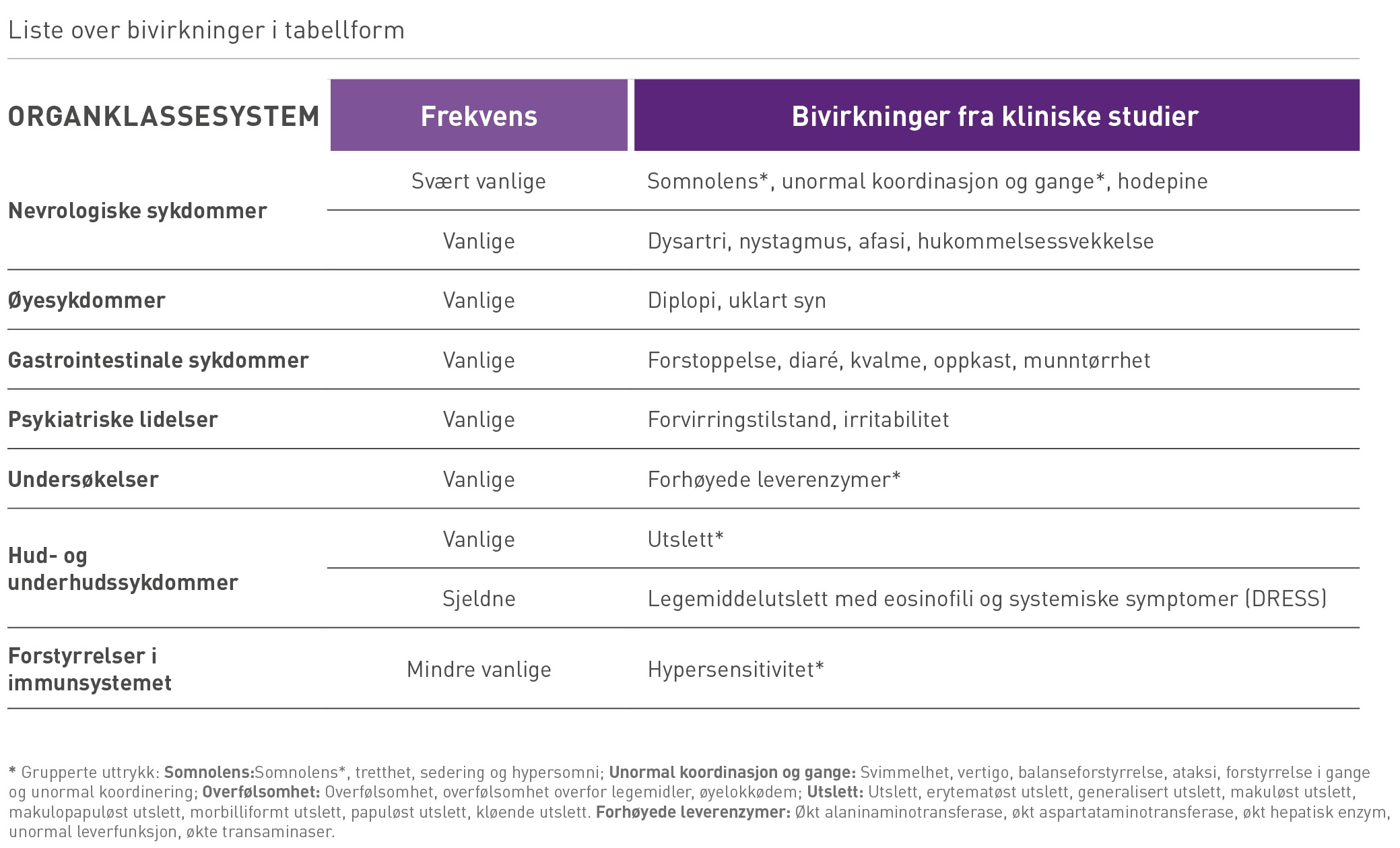
Forekomsten av bivirkninger var doserelatert.7
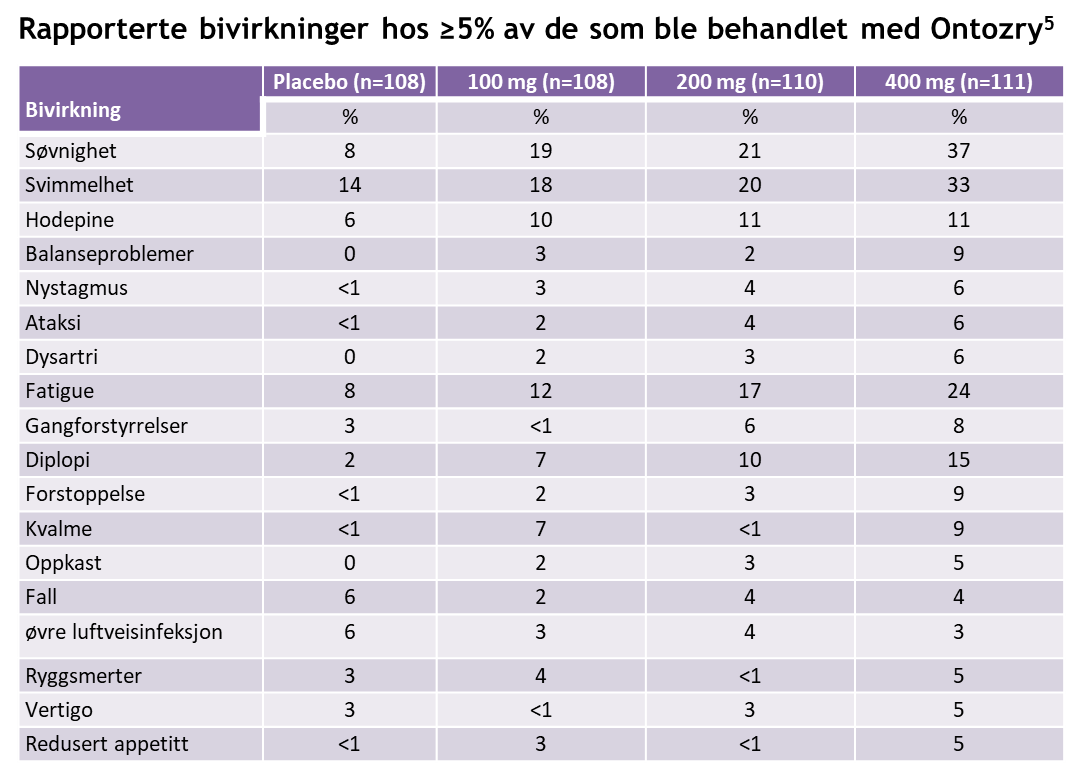
Tilpasset av Angelini Pharma fra ref. 5
Advarsler og forsiktighet
DRESS7,8
Legemiddelreaksjon med eosinofili og systemiske symptomer (DRESS), som kan være livstruende eller dødelig, er rapportert i tre tilfeller der behandling med ONTOZRY ble startet med høyere doser (50 mg eller 100 mg daglig) og titrert raskt (ukentlig eller raskere titrering). De tre tilfellene ble rapportert i løpet av 2–4 uker etter påbegynt behandling. Når behandling med ONTOZRY ble startet i henhold til anbefalt doseringsskjema med 12,5 mg/dag og titrert annenhver uke, ble det i en åpen sikkerhetsstudie med 1340 epilepsipasienter (studie C021) ikke rapportert noen tilfeller av DRESS.
Ved forskriving av ONTOZRY skal pasienter informeres om tegn og symptomer på DRESS, og overvåkes nøye for hudreaksjoner. Symptomer på DRESS er blant annet feber, utslett tilknyttet andre organsystemer, lymfadenopati, unormale leverfunksjonstester og eosinofili. Ved tegn og symptomer som tyder på disse reaksjonene, skal behandlingen med ONTOZRY stoppes umiddelbart og alternativ behandling vurderes. ONTOZRY skal alltid innledes med en dose på 12,5 mg én gang daglig og ikke titreres oftere en én gang annenhver uke.
Forkortet QT-intervall9
Familiært kort QT-syndrom er et sjeldent genetisk syndrom som er forbundet med økt risiko for plutselig død og ventrikkelarytmi, spesielt ventrikkelflimmer. ONTOZRY skal ikke brukes av pasienter med medfødt familiært QT-syndrom.
En doseavhengig forkorting av QTcF-intervallet har blitt observert med senobamat. Reduksjoner av QTcF-intervallet under 340 m/sek ble ikke observert. I kliniske studier ble det ikke funnet belegg for at kombinasjonen av senobamat og andre antiepileptiske legemidler førte til videre QTforkorting. Klinikere skal bruke varsomhet ved forskrivning av senobamat i kombinasjon med andre legemidler som er kjent for å forkorte QT.
Fertilitet, graviditet og amming10
Prevensjon for menn og kvinner
ONTOZRY anbefales ikke for fertile kvinner som ikke bruker prevensjon. Fertile kvinner som samtidig bruker p-piller, skal bruke ytterligere eller alternative ikke-hormonelle prevensjonsmidler under behandling med ONTOZRY og i inntil 4 uker etter avsluttet behandling (se Interaksjoner).
Graviditet
Risiko forbundet med epilepsi og antiepileptika generelt:
Det har blitt vist at hos barn av behandlede kvinner med epilepsi, er prevalensen av misdannelser to til tre ganger höyere enn prevalensen i den generelle befolkningen, som er ca. 3 %. I den behandlede populasjonen,
har en økning i misdannelser blitt observert ved polyterapi. Imidlertid er det ikke klarlagt i hvilken grad behandlingen og/eller den underliggende tilstanden er ansvarlig. Seponering av antiepileptiske behandlinger kan føre til forverring av sykdommen som kan være skadelig for både mor og fosteret.
Risiko forbundet med ONTOZRY:
Det finnes ikke tilstrekkelig informasjon knyttet til bruk av ONTOZRY blant gravide kvinner.
ONTOZRY skal kun brukes under graviditet når tilstanden krever at det er absolutt nødvendig at kvinnen behandles med ONTOZRY.
Amming
Det er ikke kjent om ONTOZRY og dets metabolitter skilles ut i brystmelk.
Studier på rotter har vist at ONTOZRY skilles ut i melken. Risiko for det ammede barnet kan ikke utelukkes. Som en forholdsregel bør amming opphøre ved behandling med ONTOZRY.
Interaksjoner11
ONTOZRY metaboliseres i høy grad, først og fremst gjennom glukuronidering, og i mindre grad gjennom oksidering.
ONTOZRY kan redusere eksponeringene for legemidler primært metabolisert av CYP3A4 og 2B6. ONTOZRY kan øke eksponering av legemidler primært metabolisert av CYP2C19. ONTOZRY kan redusere eksponeringen for substanser som først og fremst metaboliseres via CYP2C19. Når behandling med ONTOZRY innledes eller avsluttes, eller når dosen endres, kan det ta 2 uker å nå det nye nivået av enzymaktivitet.
CYP3A4-substrat
Dosen av legemidler som metaboliseres av CYP3A4, kan måtte økes ved samtidig bruk av ONTOZRY.
CYP2B6-substrat
Dosen av legemidler som metaboliseres av CYP2B6, kan måtte økes ved samtidig bruk av ONTOZRY.
CYP2C19-substrat
Dosen av legemidler som metaboliseres av CYP2C19, kan måtte reduseres ved samtidig bruk av ONTOZRY.

Interaksjoner med andre antiepileptika11
Fenytoin
Ingen dosejustering av ONTOZRY er nødvendig. Fenytoinkonsentrasjoner bør overvåkes under titrering av senobamat, og basert på individuell respons må fenytoindosen kanskje reduseres.
Fenobarbital
Ingen dosejustering av ONTOZRY er nødvendig. Fenobarbitalkonsentrasjoner bør overvåkes under titrering av ONTOZRY, og basert på individuell respons må fenobarbitaldosen kanskje reduseres.
Klobazam
Ingen dosejustering av ONTOZRY er nødvendig.
På grunn av mulig økt eksponering for den aktive metabolitten av klobazam (N-desmetylklobazam) som er forbundet med CYP3A4-induksjon (dannelse) og CYP2C19-hemming (eliminering), må klobazamdosen kanskje reduseres.
Lamotrigin
Doseavhengig reduksjon av lamotriginkonsentrasjoner kan forekomme ved samtidig bruk med ONTOZRY (med -21 %, -35 % og -52 % for senobamat 100 mg, 200 mg og 400 mg/dag). Basert på undergruppeanalyser av pasienter som samtidig tar lamotrigin, kan høyere doser av ONTOZRY (200–400 mg/dag) være nødvendig for å oppnå klinisk effekt ved samtidig administrering av lamotrigin. Avhengig av individuell respons må dosen av ONTROZRY kanskje økes.
Karbamazepin
Ingen klinisk relevante reduksjoner av effekt er sett i undergruppeanalyser av pasienter som samtidig tar karbamazepin, og ingen dosejustering er derfor nødvendig.
Valproat
Ingen dosejustering er nødvendig.
Lakosamid, levetiracetam og okskarbazepin
Farmakometriske analyser av data fra friske forsøkspersoner og pasienter tyder på at samtidig administrering med lakosamid, levetiracetam eller okskarbazepin ikke påvirker eksponeringen for ONTOZRY, og at ONTOZRY ikke har noen klinisk relevant effekt på eksponeringer for lakosamid, levetiracetam eller okskarbazepin.
Andre legemidler11
Orale prevensjonsmidler
ONTOZRY har vist en doseavhengig CYP3A4-induksjon. Ettersom hormonelle prevensjonsmidler også kan metaboliseres av CYP3A4, kan effekten av disse reduseres ved samtidig bruk av ONTOZRY. Fertile kvinner som samtidig bruker p-piller, bør derfor bruke ytterligere eller alternative ikke-hormonelle prevensjonsmidler.
OAT3-substrat
In vitro-studier har vist at ONTOZRY hemmer OAT3, en transportør som hovedsakelig er involvert i elimineringen av visse legemidler (for eksempel baricitinib, cefaklor, empagliflozin, penicillin G, ritobegron og sitagliptin). Samtidig administrering av ONTOZRY og legemidler som transporteres av OAT3, kan derfor føre til høyere eksponering for disse legemidlene.
Farmakodynamiske interaksjoner12
Farmakodynamiske interaksjoner kan påvirke effekten av et legemiddel og risikoen for bivirkninger. I motsetning til farmakokinetiske interaksjoner, påvirker ikke farmakodynamiske interaksjoner plasmakonsentrasjonen av et legemiddel. Interaksjonen skjer i stedet på effektnivå, for eksempel når to legemidler har lignende virkningsmekanismer.
Referenser:
- Ontozry SmPC 11/2023 section 4.1
- Ontozry SmPC 11/2023 section 5.1
- Guignet M, Campbell A and S H White. Cenobamate (XCOPRI): Can preclinical and clinical evidence provide insight into its mechanism of action? 2020;61(11):2329–2339.
- Ontozry SmPC 11/2023 section 4.2
- Krauss GL, Klein P and C Brandt. Safety and efficacy of adjunctive cenobamate (YKP3089) in patients with uncontrolled focal seizures: a multicentre, double-blind, randomised, placebo-controlled, dose-response trial. Lancet Neurology 2020;19(1):38-48.
- Chung SS, French JA and J Kowalski. Randomized phase 2 study of adjunctive cenobamate in patients with uncontrolled focal seizures. Neurology. 2020;94(22):e2311-e2322.
- Ontozry SmPC 11/2023 section 4.8
- Sperling MR, Klein P and S Aboumatar. Cenobamate (YKP3089) as adjunctive treatment for uncontrolled focal seizures in a large, phase 3, multicenter, open-label safety study. Epilepsia. 2020;61(6):1099-1108.
- Ontozry SmPC 11/2023 section 4.4
- Ontozry SmPC 11/2023 section 4.6
- Ontozry SmPC 11/2023 section 4.5
- Niu J, Straubinger RM and DE Mager. Pharmacodynamic interactions. Clin Pharmacology and Therapeutic. 2019;105(6):1395-1406.
NO22086P Feb 2024
 Harmonia Mentis Norway
Harmonia Mentis Norway